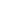格氏反应----阿拉丁试剂
发表时间:2023-12-29格氏反应是一类将烷基、烯丙基、乙烯基或芳基卤化镁(格氏试剂)加到醛或酮的羰基上的有机金属化学反应。[1,2] 该反应是有机化学中碳-碳键形成的重要工具。[3,4]
(R2也可以是氢)
格氏反应和格氏试剂由法国化学家弗朗索瓦·奥古斯特·维克多·格林尼亚(Fran?ois Auguste Victor Grignard)发现并以他的名字命名,他于1900年发表了这一研究成果[5],并因此获得1912年诺贝尔化学奖[6]。有机卤化物与镁的反应不是格氏反应,但提供了一种格氏试剂[7]。
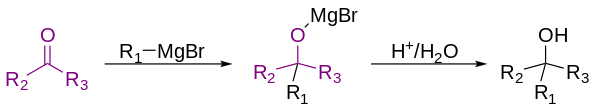
尽管格氏试剂可以引发许多反应,但经典的格氏反应仅指RMgX与酮和醛的反应,以红色显示。
反应机理
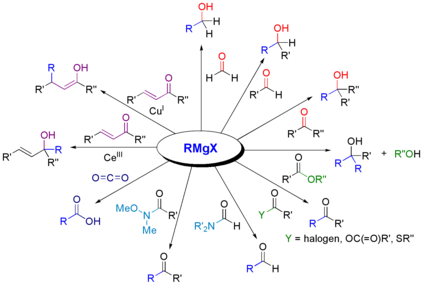
因为碳比镁的电负性更强,所以连接在镁上的碳起到亲核试剂的作用,并攻击羰基极性键内的亲电碳原子。格氏试剂向羰基的加成过程通常通过六元环过渡态进行。[8]
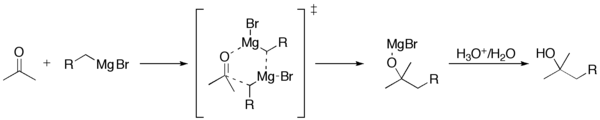
基于自由基偶联副产物的检测,还提出了另一种涉及乙烯酮自由基中间体初始形成的单电子转移(SET)机理。最近的一项计算研究表明,反应操作机理(极性与自由基)取决于底物,羰基化合物的还原电位是起决定性作用的关键参数之一。[9]
使用格氏试剂的其他反应
经典的格氏反应通常仅指酮或醛基与格氏试剂之间形成伯醇或叔醇的反应。[5] 而一些化学家将该定义理解为亲电分子与格氏试剂的所有反应。[10] 因此,当今关于格氏反应的定义依然存在一些争议。
《March's Advanced Organic Chemistry》将其定义为“将格氏试剂添加到醛和酮中……”。[1] 而《IUPAC Goldbook》中其定义却没有涉及任何一方面。[7] 在英国皇家化学学会在线发布的《Merck Index》中,经典定义得到了承认,随后是“更现代的解释拓展了格氏反应的应用范围,包括将格氏试剂添加到各种亲电底物中。” [10]
下图所示的是一些涉及格氏试剂但非经典格氏反应的有机化学反应。
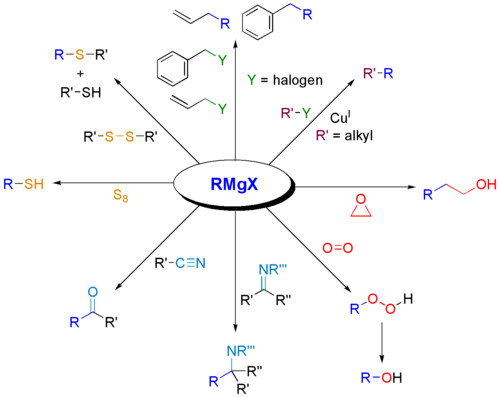
作为碱反应
格氏试剂可以用作碱,去质子化生成烯醇中间体。格氏试剂是碱性的,与醇、酚等反应生成醇盐(ROMgBr)。苯氧基衍生物易被多聚甲醛甲酰化而得到水杨醛。[17]
金属和准金属的烷基化
与有机锂化合物一样,格氏试剂也可用于形成碳-杂原子键。
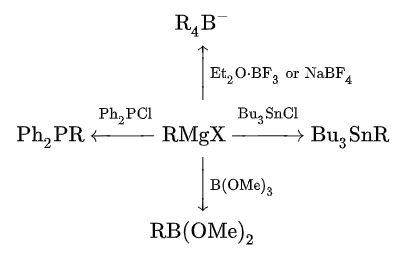
格氏试剂与许多金属基的亲电试剂反应。例如,它们与氯化镉(CdCl2)发生金属转移,得到二烷基镉。[11]
2 RMgX + CdCl2 → R2Cd + 2 Mg(X)Cl
施伦克平衡
大多数格氏反应一般都在醚类溶剂中进行,乙醚和四氢呋喃尤为常用。格氏试剂与1,4-二氧六环反应生成二有机镁化合物(R2Mg)和不溶性配位聚合物MgX2 (dioxane)2。
2 RMgX + dioxane ? R2Mg + MgX2(dioxane)2
该反应利用了施伦克平衡,将其向右侧推进。
氧化镁的前体
格氏试剂与有机锂化合物反应生成ate络合物(Bu = 丁基)。[12]
BuMgBr + 3 BuLi → LiMgBu3 + BuBr
与有机卤化物偶联
格氏试剂通常不与有机卤化物反应,这与它们和其他主族卤化物的高反应性形成了鲜明的对比。但在金属催化剂存在条件下,格氏试剂可参与C-C偶联反应。例如,酯类在用NaOH碱性条件下水酯后,在Fe(acac)3的存在下,壬基溴化镁与对氯苯甲酸甲酯反应,得到对壬基苯甲酸,如下所示。如果没有Fe(acac)3的存在,格氏试剂则会攻击芳基卤化物上的酯基。[13]
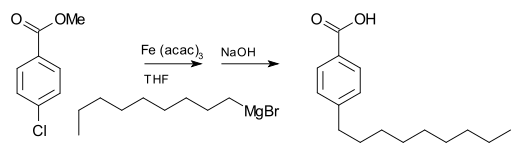
对于芳基卤化物与芳基格氏试剂的偶联反应,氯化镍的四氢呋喃(THF)溶液也是一种高效的催化剂。此外,混合氯化锂(LiCl)和氯化铜(CuCl2)制备的Gilman催化剂四氯铜酸锂(Li2CuCl4)四氢呋喃溶液是一种有效的烷基卤化物偶联催化剂。Kumada-Corriu耦合提供了取代的苯乙烯。
工业应用
格氏反应的一个工业应用实例是苯基溴化镁参与用于治疗雌孕激素受体表达阳性的抗乳腺癌药物他莫昔芬工业化生产。[14,15]

参考文献
1. Smith, Michael B.; March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th ed.),New York:Wiley-Interscience,ISBN 978-0-471-72091-1
2. Chapter 19: Carboxylic Acids. Organic Chemistry 4e Carey. mhhe.com
3. Shirley, D. A. (1954). "The Synthesis of Ketones from Acid Halides and Organometallic Compounds of Magnesium, Zinc, and Cadmium". Org. React. 8: 28-58.
4. Huryn, D. M. (1991). "Carbanions of Alkali and Alkaline Earth Cations: (ii) Selectivity of Carbonyl Addition Reactions". In Trost, B. M.; Fleming, I. (eds.). Comprehensive Organic Synthesis, Volume 1: Additions to C-X π-Bonds, Part 1. Elsevier Science. pp. 49-75. https://doi.org/10.1016/B978-0-08-052349-1.00002-0
5. texte, Académie des sciences (France) Auteur du (January 1, 1900). "Comptes rendus hebdomadaires des séances de l'Académie des sciences/publiés. par MM. les secrétaires perpétuels". Gallica. Retrieved April 23, 2023.
6. Grignard, V. (1900). "Sur quelques nouvelles combinaisons organométaliques du magnésium et leur application à des synthèses d'alcools et d'hydrocabures". Compt. Rend. 130: 1322-25.
7. IUPAC. Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). Compiled by A. D. McNaught and A. Wilkinson. Blackwell Scientific Publications, Oxford (1997). ISBN 0-9678550-9-8. https://doi.org/10.1351/goldbook
8. Maruyama, K.; Katagiri, T. (1989). "Mechanism of the Grignard reaction". J. Phys. Org. Chem. 2 (3): 205–213. https://doi.org/10.1002/poc.610020303
9. Peltzer, Raphael Mathias; Gauss, Jürgen; Eisenstein, Odile; Cascella, Michele (February 12, 2020). "The Grignard Reaction-Unraveling a Chemical Puzzle". Journal of the American Chemical Society. 142 (6): 2984–2994. https://doi.org/10.1021/jacs.9b11829
10. "Grignard Reaction | The Merck Index Online". www.rsc.org. Retrieved April 23, 2023.
11. "Unit 12 Aldehydes, Ketones and Carboxylic Acids". Chemistry Part II Textbook for class XII. Vol. 2. India: National Council of Educational Research and Training. 2010. p. 355. ISBN 978-81-7450-716-7. Archived from the original on September 20, 2018. Retrieved March 9, 2019.
12. Arredondo, Juan D.; Li, Hongmei; Balsells, Jaume (2012). "Preparation of t-Butyl-3-Bromo-5-Formylbenzoate Through Selective Metal-Halogen Exchange Reactions". Organic Syntheses. 89: 460. https://doi.org/10.15227/orgsyn.089.0460
13. A.Fürstner, A. Leitner, G. Seidel (2004). "4-Nonylbenzoic Acid". Organic Syntheses. 81: 33–42.
14. Richey, Herman Glenn (2000). Grignard Reagents: New Developments. Wiley. ISBN 0471999083.
15. Jordan VC (1993). "Fourteenth Gaddum Memorial Lecture. A current view of tamoxifen for the treatment and prevention of breast cancer". Br J Pharmacol. 110 (2): 507–17. https://doi.org/10.1111/j.1476-5381.1993.tb13840.x
阿拉丁提供相关产品,详情请见阿拉丁官网:https://www.aladdin-e.com/zh_cn/faq/technical-articles/Grignard_reaction/